文|氨基观察
11月16日,注定是生物技术发展的一个新的里程碑。
当日,英国正式批准福泰制药与CRISPR Therapeutics共同研发的基因编辑药物Casgevy上市申请。由此,Casgevy成为全球第一个上市的CRISPR基因编辑疗法。
这意味着,经过了十多年的漫长远征,CRISPR基因编辑疗法终于等到了曙光,医学届也将有能力,通过CRISPR技术进一步打开基因编辑世界的大门,从而治疗更多遗传病。
“基因组编辑很特别,它可能会重新定义未来30-40年的医学范式。Casgevy的批准代表了它的开始。”CRISPR Therapeutics的首席执行官Samarth Kulkarni博士对此说道。
一夜之间,基因组编辑疗法的竞争来到了新起点。
/ 01 / “基因魔剪”新时代
基因编辑领域的发展,依赖于“编辑工具”。
毕竟,基因编辑的核心,是对生物体基因组特定目标基因,进行修饰、改造。因此,对于科学家们来说,一个衬手的“编辑工具”至关紧要。
而CRISPR基因编辑,正是这样一款技术工具。
CRISPR-Cas系统原本是原核生物的一种天然免疫系统。某些细菌在遭到病毒入侵后,会将病毒的一小段基因,存储到一个称为“CRISPR”的存储空间。
当该细菌再次遇到相同的病毒入侵时,它能靠“记忆”识别病毒,并派出“工兵” Cas蛋白(有多种蛋白,Cas9即为代号9的蛋白),根据记录的基因片段,在相应位置剪断病毒DNA,从而歼灭病毒。
CRISPR-Cas系统的诞生,让基因编辑从直板机步入智能机时代。相比此前的ZFN、TALENs基因编辑技术,CRISPR-Cas系统有三大显著优点:操作简单、精准度高、花费便宜。
手起刀落、快准狠,CRISPR-Cas9有着“基因魔剪”之称。知乎上,便有博士生打趣道,以前用TALENs技术KO斑马鱼,靶点不好选,效率也一般,要6-7年才能毕业;自从有了基因魔剪,一打一个准,5-6年就能毕业了。
更权威的认可,则是2020年诺贝尔化学奖,颁给了为CRISPR技术作出贡献的科学家。
过去十年,该技术已在全球无数生物实验室落地开花,在医学领域有着极高的潜力。
全世界有超过7000种罕见病,病患人数超过3亿人,其中80%是单基因突变造成的。而目前95%的罕见病仍没有有效的治疗药物。
利用基因编辑技术,对发生突变的单个碱基进行剪断、加入或替换等修正操作,就极有可能挽救罕见病人的生命,还他们健康。
理论上,任何突变的基因都可以通过CRISPR-Cas系统纠正。如今,Casgevy的上市,正式意味着这一时代的开启。
/ 02 / Casgevy的魔力
尽管仍缺乏完整和全面的临床数据,但某种程度上,Casgevy已经证明了其潜力。
Casgevy的核心机制,是借助CRISPR基因编辑手段,改造患者自身的造血干细胞,让细胞能产生高水平的胎儿血红蛋白。
通常来说,胎儿血红蛋白只会在胎儿发育过程中产生,出生后它的表达通路会被关闭。但某些特殊案例显示,当BCL11A基因突变时,一些成年人也能生成胎儿血红蛋白。
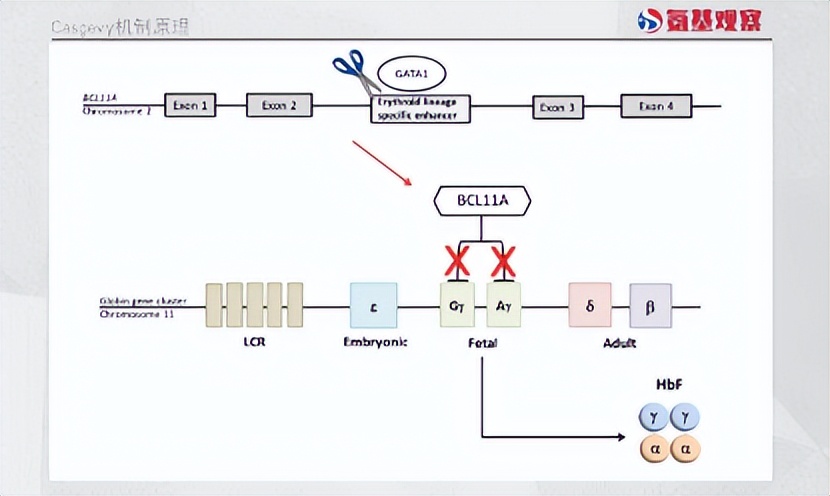
Casgevy做的就是模拟这种突变,让患者造血干细胞的BCL11A进行切割,松开胎儿血红蛋白的刹车。这也使得,Casgevy具有治疗镰状细胞病、输血依赖性β地中海贫血的潜力。
在镰状细胞病的临床试验中,目前有45名患者接受了Casgevy治疗。其中29名提供足够成熟的患者数据显示,28例在治疗后至少12个月内,没有出现严重疼痛迹象。
而在输血依赖性地中海贫血β的临床试验中,目前有54名患者接受了Casgevy治疗。基于42名成熟患者的数据显示,39例在治疗后至少12个月内不需要输注红细胞,另外3名患者对红细胞输注的需求减少了70%以上。
从短期安全性方面来看,副作用通常与自体干细胞移植一致。这些数据无疑表明,不管是针对镰状细胞病还是输血依赖性地中海贫血,Casgevy都具有一定的竞争力。
/ 03 / 完成的与未完成的
Casgevy的上市,对于CRISPR编辑技术来说,还只是新时代探索的开始。
对于Casgevy本身来说,治疗的繁琐复杂与成本高昂的痛点,将是考验其商业化前景的因素。
治疗方式层面,Casgevy首先需要通过从患者的骨髓中取出干细胞,并在实验室中编辑细胞然后进行回输。在回输之前,还要消除掉骨髓中原本的天然造血干细胞,以减少后续异常血红蛋白的表达,并为新造血干细胞的生长留出空间。
在回输之后,患者可能需要在医院观察至少一个月,以避免潜在的感染等问题。
与此同时,Casgevy的定价也很关键。根据非营利组织临床和经济评论研究所的一份报告,如果该疗法获得批准,预计价格将极其昂贵,每位患者的费用可能高达200万美元。如此高昂的治疗费用,很可能将绝大部分的患者阻挡在外。
繁琐的步骤、高昂的成本,是Casgevy需要面对的挑战。而CRISPR编辑技术的前进方向,则取决于长期安全性问题,以及是否能够从体外编辑转化为体内编辑等。
其中,最为关键的必然是长期安全性问题。自2012年CRISPR基因编辑技术诞生以来,脱靶变成为其发展制约的主要因素之一。如果CRISPR基因编辑技术对预期靶标以外的其他DNA片段进行了切割,可能会破坏非靶向基因的功能或调节,引发严重后果。
为了确定Casgevy脱靶的分析是否可靠,FDA不久前还召集了智囊团开会表决。虽然在会议上,专家小组对该药物的安全性表示肯定,但仍需要药企后续更长周期的临床数据来证明。
CRISPR基因编辑技术还很年轻,未来还有很长的路要走。但毋庸置疑的是,Casgevy的上市将成为基因编辑疗法的历史性时刻,一个新的时代已经拉开序幕。
国内药企也不会缺席。当前,包括博雅基因、和度生物、天泽云泰、微光基因等均参与这一新时代的角逐。或许,不远的将来,国内药企也会带来好消息。



评论