昨天也许是人类“征服”自然的历史上又一个具有里程碑意义的日子。但这个日子来得有些草率,在没有任何预兆的情况下,来自中国深圳的科学家贺建奎向世界宣布,一对名为露露和娜娜的基因编辑婴儿已于今年11月顺利降生。他的团队通过“CRISPR/cas9”基因编辑技术,对这对双胞胎的CCR5基因进行了修改,修改后的基因使她们具备了对艾滋病这一世纪顽疾的天然免疫力。
随着越来越多的细节被媒体陆续披露出来,整个事件越来越像是一个科幻故事的开头:最初在网上曝光的一份“医学伦理委员会审查申请书”是由深圳和美妇儿科医院出具的,但这家医院随后表示“基因编辑婴儿未在本院出生”,在“申请书”上签字的伦理委员会成员也对申请书的真实性提出了质疑。而贺建奎所在的南方科技大学则发布公告称,贺建奎已于2018年2月停薪留职,校方对他正在进行基因编辑临床试验一事并不知情。更可怕的是,据“果壳网”报道,参与临床试验的家庭是否完全理解实验目的以及潜在风险,我们也不得而知,因为给参与者的知情同意书上将这一项目描述为“艾滋病疫苗研发计划”。而这个故事的恐怖之处正在于,接下去情节该怎么发展,现在还没人知道。
在基因编辑的领域里,是否已经有人代表人类打开了潘多拉的魔盒?从基因治疗到基因编辑,过去30年我们已经走过了怎样的历史?从治疗到预防,贺建奎团队迈出了多么冒险的一步?从预防到改善,人类离可以“挑选”基因、“订制”后代的未来还有多远?从“生人”到“做人”,迈克尔·桑德尔、哈贝马斯与弗朗西斯·福山对这一技术的思考,是如何处理形而上层面基因编辑对自由与人性的影响的,又面临着怎样陈词滥调的风险?
1、从基因治疗到基因编辑:一个曲折的“抗艾”故事
通过修改CCR5基因的方法来对抗艾滋病,早不是什么新鲜事了。浙江大学生命科学研究院教授王立铭在《上帝的手术刀:基因编辑简史》一书中就提到了著名的“柏林病人”案例。

1995年,德国人蒂莫西·雷·布朗(Timothy Ray Brown)被确诊为艾滋病,2006年,不幸再次降临在他身上,这次是致命性的急性髓细胞性白血病。但出人意料的是,这两种致命疾病的接连打击反而给了布朗重获新生的机会。

其中的原委要从艾滋病的病因说起。艾滋病源于人体免疫缺陷病毒(简称“HIV”)的感染。HIV能够精准地识别人体内的某一类免疫细胞,入侵并杀死这些细胞,从而令患者丧失免疫机能,最终死于严重的感染。而在HIV入侵免疫细胞的过程中,需要借助免疫细胞表面的一些“路标”蛋白来指明方向,这些蛋白中就包括一个名为“CCR5”的蛋白。全世界大概有1%的人口(多为北欧白人)对艾滋病具有天然免疫力,就是因为编码CCR5蛋白的基因在他们身上发生了功能突变,导致这个“路标”无法被HIV识别。
正是基于这一原理,布朗的主治医生提出了一个破釜沉舟、一石二鸟的解决方案,即在彻底清除掉布朗体内携带HIV病毒同时又已经癌变的骨髓细胞之后,再选择CCR5基因变异的骨髓捐献者,给布朗进行骨髓移植,这样就可以同时治愈他身上的两种绝症。这个大胆的方案最终果然让布朗奇迹般地幸存了,也让他成为了迄今为止唯一一个被彻底治愈了的艾滋病患者。

但医生为布朗制定的治疗方案并不属于“基因编辑”,而是“基因治疗”,他并没有直接对布朗的基因进行修改,而是给他体内引入了其他的基因。“基因治疗”技术自上世纪90年代初开始被应用于人体,主要用于治疗一些罕见的“单基因遗传病”,这些疾病是由于单个基因的DNA序列和功能发生变异而导致的。王立铭在书中指出,从1990年算起,全世界通过基因治疗重获健康的幸运儿不超过千人,我们在科学杂志和媒体上看到的,更多是基因治疗领域反复出现的临床事故和失败案例。在1990年之后的10年间开展的超过500个基因治疗临床试验全部以失败告终,没有一项疗法最终顺利进入大规模临床应用的阶段。王立铭将这十年称作基因治疗“喧嚣和泡沫的十年”,站在今天回望,那就是“革命性的概念突破和随之而来的巨大商业利益驱动的一场大跃进”。
基因治疗的逻辑就是简单的“缺啥补啥”,即给患者体内引入一段具有正常功能的基因序列。但其技术壁垒在于,如何把一个特定的DNA序列放回到人体细胞里。当时普遍的做法是利用病毒作为基因的“搬运工”,但问题在于,病毒除了运输基因的天才本领,还会在人体内悄悄地做很多事情,其中有一些无伤大雅,另一些则会要人命。当时的几百个临床试验,就是败在了这些暗地里捣鬼的“搬运工”手上。
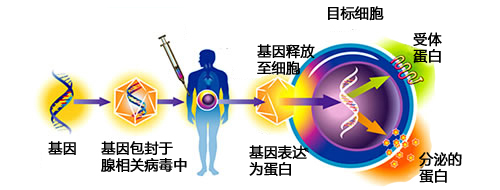
既然“缺啥补啥”不能解决问题,科学家于是将目光转向了对人类的遗传物质本身进行修改的新思路上,“基因编辑”的概念就此应运而生。与传统的基因治疗不同,基因编辑的逻辑在于通过某种外科手术式的操作,精确修复出现遗传变异的基因,从根本上阻止遗传疾病的发生。与基因治疗相比,它的优势非常明显。简而言之,基因编辑能解决传统的基因治疗所解决不了的问题,即便是基因治疗能解决的问题,它也能解决得更精确、更漂亮。
2014年底,宾夕法尼亚大学医学院的一群医生在《新英格兰医学杂志》上发表论文,称借助来自圣加蒙公司(Sangamo Therapeutics)的技术平台,他们正利用锌手指核酸酶改造人体免疫细胞,试图治疗世纪顽疾艾滋病。他们的思路和前文故事里的”柏林病人“如出一辙,即通过精确地破坏掉艾滋病患者体内免疫细胞的CCR5基因来治疗艾滋病。由于美国科学规范和医学伦理的严格要求,第一期临床试验的主要目的是检验相关治疗方案的安全性,而不是疗效。论文指出,对于参与了一期临床试验的12名艾滋病患者,医生们主要证明了针对CCR5基因的基因编辑疗法对他们是安全的。
回到中国深圳这对双胞胎的例子,它的“突破”主要在于,将基因编辑技术的应用从“治疗”推进到了“预防”。但在这个案例中,这样激进的“预防”真的有必要吗?王立铭昨天在某知识付费平台发表文章认为,对这一个案而言,基因编辑的风险远远大于收益。他在文中提到,据美联社报道,双胞胎的母亲并非艾滋病患者,父亲虽然是艾滋病毒携带者,但在长期治疗后得到了很好的控制,在这样的情况下,母亲只需在孕期注意防护,孩子100%不会受到艾滋病毒感染。而孩子出生之后,感染艾滋病的风险也是完全可控的,即便真的不幸染病,目前的医疗手段也已经将艾滋病变成了慢性病,并不影响患者的寿命。
也就是说,基因编辑对于这对双胞胎而言收益几乎可以忽略不计,相反,其风险却难以估量。贺建奎团队采用的CRISPR/cas9技术,是目前被广泛研究和应用的一项基因编辑技术,但它仍然有很多根深蒂固的风险没有解决。其中最主要的风险就是难以避免的“脱靶”效应,简单地说,CRISPR/cas9技术在应用时,可能会破坏人体中原本正常的无关基因,从而给患者带来严重的、难以预计的遗传病风险。除此之外,由于基因编辑是在受精卵中进行的,这些修改后的基因很可能会进入婴儿的所有细胞——包括生殖细胞,这就意味着,这次基因编辑的结果不单会影响两个婴儿本身,还会传递给她们的子孙后代。
2、从“治疗”到“改善”:基因编辑的伦理边界在哪里?
除了对个案的风险评估之外,王立铭还谈到了更大的担忧,一旦“治疗”和“预防”的边界被打破,那么从“预防”到“改善”的底线又还能守住多久呢?事实上,人类可以“挑选”基因、“订制”后代的场景已经在科幻小说和哲学著作中被反复想象和演练过了。
法国哲学家吕克·费希(Luc Ferry)在《超人类革命:生物科技将如何改变我们的未来?》一书中就将这些模糊了“治疗”和“改善”边界的实践称为“超人类主义运动”。他指出,超人类主义是利用科学进步(尤其是生物技术的进步)对当前人类的体能、智力、情感和道德等方方面面进行改造的大工程。它最本质的特征,就是从传统的“治疗模式”到“改善模式”(或者说是“增强模式”)的跨越。

在超自然主义者们看来,实现这种“从运气到选择”的转变是完全合理的,甚至是一种道德义务。因为在今天的世界,所谓的“分配正义”只能通过补偿的方法来解决不平等的问题。这种不平等一部分可以归因为“社会彩票”(种族、性别、阶级、宗教等),另一部分则源于“自然彩票”(健康、天赋等),对于后者,我们至今无可奈何,只能采取“外部干涉”,具体的手段包括金钱补偿、免费医疗、特殊教育等等,而基因技术则赋予了我们“纠正”这种自然的不平等的能力。
除此之外,超自然主义者拒绝被与臭名昭著的优生学划等号,他们强调,优生学是一种国家主导的带有强制性的集体实践,而基因编辑则是一种个体自由,它的目的不是消灭弱者或者“怪胎”,而是纠正盲目而冷漠的自然对人类造成的不公,最终实现“基因平等”。
美国政治哲学家、哈佛大学教授迈克尔·桑德尔(Michael J. Sandel)在《反对完美:科技与人性的正义之战》一书中也谈到了这种所谓的“自由主义优生学”,他举了一个与基因编辑技术无关的例子来说明“订制后代”的伦理困境。美国的一对女同性恋伴侣决定要一个孩子,她们两人都失聪,并以此为傲。她们认为耳聋是一种生活方式,甚至是一种文化认同,而并非是一种需要被治疗的残疾。她们也想要生一个失聪的孩子,希望“跟孩子分享聋人群体美好的一面”,于是找来了一个上溯五代都是聋人的精子捐献者,果然,她们如愿以偿了,孩子天生失聪。

《华盛顿邮报》报道了她们的故事之后,谴责声铺天盖地而来,在大多数“健康人”看来,她们这样做,是“蓄意”将残疾加诸于孩子身上,但两人辩称,她们只是想要一个像自己一样的孩子而已,而这种心态“和大多数健康的异性恋伴侣生孩子时的想法没什么不同”。
桑德尔借此提出了一个问题,“订制”一个先天失聪的孩子是错的吗?如果是的话,那是错在失聪的部分,还是订制的部分呢?在桑德尔看来,一旦人们拥有了“订制”的权力,“治疗”和“改善”之间的边界就会变得非常脆弱。因为“健康”并不完全是一个生物学问题,或者说它没有一个标准答案。在这个案例中,分歧就在于,耳聋究竟是一种需要被治疗的残疾,还是一种身份认同?
更多的时候,人们纠结于“多健康才算是健康”这个无止境的问题。如果一个人会因为体内的一个基因变异,增加1%患某种疾病的风险,他需不需要去做基因编辑?如果将这个概率缩小到千分之一或万分之一呢?很多时候,人们对健康的理解是功利性的,健康之所以被珍视,并不在于其本身的价值,而在于它可以作为一种资源、一种实现其他目的的手段。桑德尔认为,健康并不是那种可以被价值最大化的优点,没人渴望成为健康大师,健康是“有止境”的,不必冒着卷入优生“军备竞赛”的风险,父母就足以让孩子健康。
3、从“生人”到“做人” :形而上学如何帮我们思考技术?
基因工程作为一种“私有化”的、“自由市场”的优生学,尽管褪去了20世纪初优生学的“国家强制性”,将选择权交到了父母手上,但同时,也将彻底破坏现有的亲子关系,破坏建立在父母对孩子无条件的爱和养育这一规范之上的种种社会实践。桑德尔援引德国哲学家、社会学家哈贝马斯(Jürgen Habermas)的观点,认为基因编辑将会导致父母对孩子的爱的工具化,让亲子之间发展出一种设计者与被设计者的从属关系,也会衍生出新的责任与义务。
哈贝马斯在《人性的未来:走向自由优生学?》一书中还谈到了一个更为形而上学的观点,他认为,所谓的“自由优生学”其实是反自由的,或者说它彻底让自由成为了不可能。哈贝马斯指出,“我们感受自由时,都会有个参考依据,这个参考依据就其本质而言,不能是经过安排的。”也就是说,如果我们是自由的,那么我们必须将自己的存在(或者说出生)归因于一个“排除人为干预的开始”,一个“神或自然,而不是其他人安排的起点”。“出生”是一个自然的事实,这是人类自由的基础。

哈贝马斯认为,这一观点在西方哲学史上鲜少有人讨论,但他在汉娜·阿伦特(Hannah Arendt)的著作中发现了一个类似的论述,阿伦特将“出生”——即把人类“生出来”而不是“做出来”的事实——看作是他们具有采取行动的能力的先决条件。“非人为安排的生命开始的偶发性,与赋予人类生命道德形态的自由之间是有联系的,”哈贝马斯这样断言。
然而,一旦脱离了具体操作层面的伦理探讨,上升到形而上学的高度,反对基因编辑的声音就很容易落入西方传统的本质主义、人类中心主义的窠臼。弗朗西斯·福山(Francis Fukuyama)的《我们的后人类未来:生物技术革命的后果》一书就充满了这样的陈词滥调:
“我们需要继续感知痛楚,承受压抑或孤独,忍受令人虚弱的疾病折磨,因为这是人类作为物种存在的大部分时段所经历的。”
“人性的保留是一个具有深远意义的概念,为我们作为物种的经验提供了稳定的延续性,它与宗教一起,界定了我们最基本的价值观。”
“我们试图保存全部的复杂性、进化而来的禀赋,避免自我修改。我们不希望阻断人性的统一性或连续性,以及影响基于其上的人的权利。”
问题在于,福山口中所谓的“人性”、“价值观”、“人的权利”并非是人类历史上一以贯之的,更谈不上是什么不可修改的本质,它不仅只属于特定的历史阶段,而且是极端西方中心的。他试图通过“人与非人”、“自然与人工”这样简单的二元对立来反对经过基因编辑的人,但同样的二元对立在历史上也曾经被用于反对女性、反对有色人种、反对动物、反对一切“他者”。这一思想本身,和技术乐观主义者(或者叫做解决问题主义者)同样傲慢,同样会指向一种霸权。

在技术日新月异的今天,对于技术的反思和批判,需要的是新的理论、新的认识框架、新的知识生产机制。人文学科作为新技术潜在伦理与道德风险的最后一道防线,再祭出这样生了锈的“冷兵器”,无异于螳臂当车了。
参考文献:
《上帝的手术刀:基因编辑简史》(王立铭 著,湛庐·浙江人民出版社,2017-05)
《超人类革命:生物科技将如何改变我们的未来?》(吕克·费希 著,周行 译,湖南科学技术出版社·读行者,2017-10)
《反对完美:科技与人性的正义之战》(迈克尔·桑德尔 著,黄慧慧 译,中信出版社,2013-05)
《我们的后人类未来:生物技术革命的后果》(福山 著,黄立志 译,理想国 | 广西师范大学出版社,2017-01)





评论