文|未来迹FutureBeauty 《未来迹》向婷婷
近日,国家市场监督管理总局缺陷产品管理中心网站发布信息,新基石(深圳)科技有限公司按照《消费品召回管理暂行规定》的要求,主动向国家市场监督管理总局报告了召回计划:
将召回2020年3月至2021年9月期间进口的初普牌第一代Stop Eye型号家用射频美容仪,涉及数量共182215台。按其每台1500元左右的零售价格测算,召回产品总价值达2.7亿元以上。
存烫伤风险,美容仪成“毁容仪”?
公告显示,本次召回的初普一代家用射频美容仪,如果在使用过程中长时间停留在同一位置或过于缓慢移动时,可能出现设备探头温度过高的现象,极端情况下存在导致皮肤烫伤的安全隐患。
对于这批被召回产品,新基石(深圳)科技有限公司将为消费者免费维修,增加温控器,并在官方网站发布产品安全使用视频,以消除安全隐患。
当前,公司主动召回的初普牌第一代Stop Eye家用射频美容仪已经无法在天猫、京东等旗舰店搜索到。根据社交媒体上的用户内容显示,初普天猫官方旗舰店回应用户:此次主动召回计划,目的是进一步提升用户体验,防止消费者的错误使用以及错误使用可能带来的风险。
“第一代Stop Eye家用射频美容仪是安全而有效的,目前我们没有收到任何消费者在正确使用仪器的情况下而造成肌肤不良反应投诉。”初普天猫客服向消费者这样表示。
专家介绍,射频美容仪的工作原理,是将射频能量传递到皮肤的真皮层,使真皮层温度达到45-50摄氏度。在这个温度下,胶原纤维收缩,同时刺激胶原蛋白新生,起到紧致皮肤、改善细纹的效果。因此,温度的控制对射频美容仪极为重要。
然而,这并非初普的首次翻车,此前初普就因为温控问题被诟病。
去年315国际消费者维权日,中国家电网与中国检验检疫科学研究院联合开展了“家用美容仪比较试验”,对市面上的8款射频美容仪进行了温度、电器安全等方面的检测。其中,初普美容仪TriPollar Stop EYE测试不达标,在使用时温度最高超过60℃,完全超出人体承受温度,存在很大程度的烫伤风险。
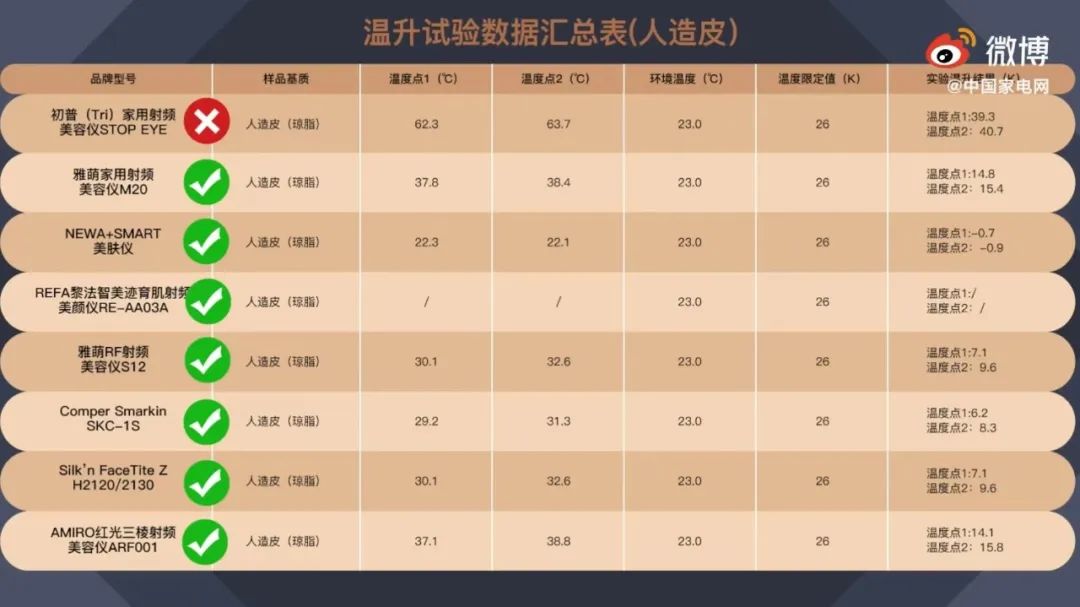
而对于以上机构的测评结论,初普TriPollar却认为,“极限测试”不能作为射频美容仪安全性的评价依据。
但一家国内美容仪品牌负责人告诉《未来迹Future Beauty》:
“美容仪作用于人体面部,面部又分为表皮层和真皮层,一般来说,真皮层在55-65°C时,能刺激胶原新生,在安全范围内,美容仪(射频仪)的输出能量越高,效果越好。但对于表皮层来说,安全临近值为43°C,超过这个温度,就有被低温烫伤的风险,因此现在许多美容仪会内置温控系统,保证产品安全。”
3大问题频发:爆发式增长下的美容仪赛道
近年来,电子美容仪不仅从小众市场走到了大众消费市场,也迎来了向高端化的转变。
根据《GfK2021年电子美容仪市场总结》的数据显示,电子美容仪市场结构在过去3年中发生了巨大的变化,拥有“医美”效果的高端美容仪产品带动了3000+价格段市场的快速增长。2021年,3000元以上价格段的市场销售额超过38亿元,较2020年有17.8%的增长。相反,3000元以下的美容仪市场份额在过去几年中呈持续下降的趋势。
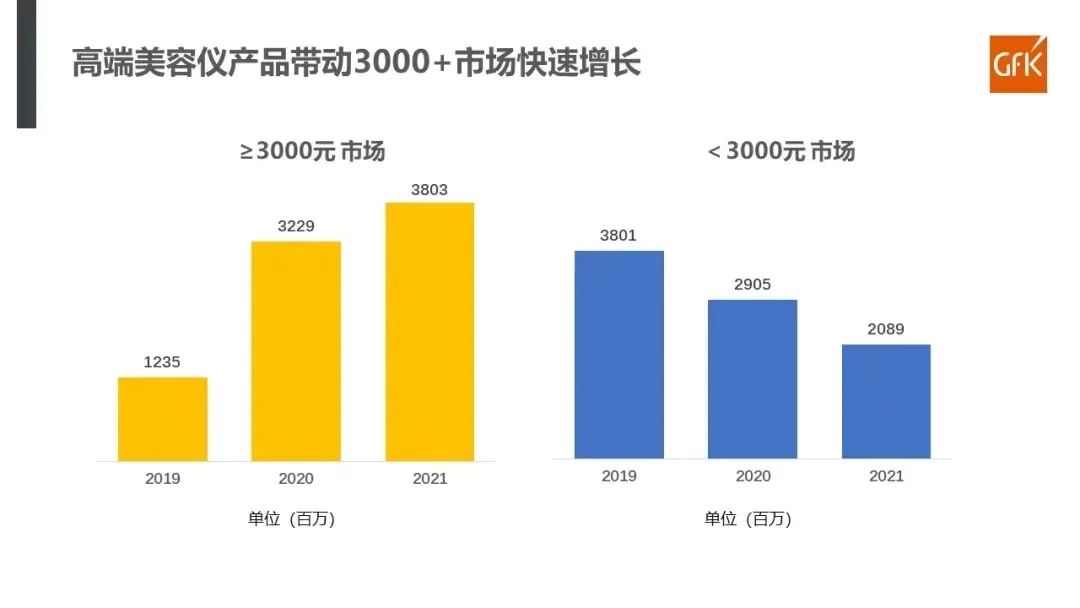
然而,在爆发式增长的背后,美容仪赛道也问题频发。主要问题有3类:低温烫伤、重金属超标和虚假宣传。
初普此前因涉及虚假宣传处于风口浪尖。此前,初普TriPollar美容仪的Stop Eye和Stop Vx在商品详细中,称产品具有欧盟CE认证、FDA技术认证。“FDA认证”被质疑后,初普方一边将此事定性为翻译失误造成,而另一边又撤下了各销售平台的“FDA认证”。
而后,超头公司“美腕(上海)网络科技有限公司”被罚款30万元,原因是超头在直播中推广初普stop vx美容仪时,“使用误导消费者的宣传用语”。
2020年10月18日,央视《每周质量报告》节目推出了家用美容仪质量的报道。
节目中测试了市面上销售量较高的10款美容仪,发现2款产品存在低温烫伤风险、6款产品存在着镍释放量超标的情况,甚至有的产品镍金属超出欧盟标准近40倍。镍是一种最常见的致敏金属,长期或反复地使用镍释放量不符合要求的产品易引起过敏症状,严重的还会造成身体伤害。
产品存在安全隐患、虚假功效宣传、过度营销、山寨品牌侵权……美容仪赛道在快速扩张的同时,市场乱象亟需整顿。
法规跟进,2年后美容仪将迎来“最严”监管
“市场发展太快,而相关法律法规和官方标准都没跟上,就直接导致了市场乱象。”上述美容仪品牌负责人认为,美容仪市场发展速度过快,行业监管却仍待跟进。
据了解,目前在国内现行标准中,涉及家用美容器具产品的标准有3项,分别是:GB4706.15-2008《家用和类似用途电器的安全皮肤及毛发护理器具的特殊要求》、GB4706.85-2008《家用和类似用途电器的安全紫外线和红外线辐射皮肤器具的特殊要求》和GB/T36419-2018《家用和类似用途皮肤美容器》。
2021年4月,国家药监局发布关于征求《射频美容类产品分类界定指导原则》(征求意见稿)(下称:《原则》)意见的通知,以规范在医疗器械领域中射频美容类产品的分类界定,并为产业和监管部门提供注册和审批的技术指导。对美容仪市场的监管迈出重要一步。
《原则》中,将三类射频美容仪纳入医疗器械管理,并根据射频美容类产品的风险程度,其管理类别应不低于Ⅱ类医疗器械管理。
另根据我国《医疗器械监督管理条例》规定,第三类医疗器械是植入人体;用于支持、维持生命;对人体具有潜在危险,对其安全性、有效性必须严格控制的医疗器械,生产第三类医疗器械,应当通过临床验证,临床验证应当在省级以上人民政府药品监督管理部门制定的医疗机构进行。
也就是说,在2024年射频美容仪被纳入三类医疗器械管理后,相应的功效验证也必须到位。
从家用电器到医疗器械,对射频美容仪的管理正在逐步迈向规范化。但对于正快速发展且种类繁多的美容仪行业而言,现行生产标准在“过渡期”仍然亟需完善。



评论