文|氨基财经
创新药的赛道从来不缺突破。
从1960年双抗概念首次提出到2021年年底,近六十多年时间双抗领域仅有卡妥索单抗、博纳吐单抗、艾美赛珠单抗、Rybrevant四种产品上市,其中卡妥索单抗因表现不佳退市。(PS:根据此前抗体药物命名规则,双抗产品的后缀也是单抗)
与单抗、ADC、CAR-T等热门赛道的百家争鸣相比,双抗赛道似乎要冷清许多。不过,风水轮流转,如今寂静了几十年的双抗赛道,终于起风了。
8月24日,强生的双抗药物Tecvayli在欧盟获批上市,这是全球首个靶向BCMA/CD3的双抗药物,也是今年获批上市的第五款双抗。
仅用一年的数据,双抗获批数量已经超越此前总和。之后,又会发生什么呢?
BCMA/CD3双抗,多发性骨髓瘤患者的新希望
近年来,虽然创新药频出,但距离我们真正征服肿瘤,还有很长的路要走。
例如,相对容易攻克的血液瘤领域,多发性骨髓瘤有效治疗手段依然稀缺。在现有治疗手段之下,几乎所有患者都会复发,需要接受后续治疗。但是,对于复发后的骨髓瘤患者,我们仍然没有太好的治疗方案。
但总体来说,肿瘤药物的进步有目共睹。如今,双抗的兴起给多发性骨髓瘤患者带来了新的希望。
8月24日,强生的Tecvayli双抗获批,成为首款用于治疗复发/难治性多发性骨髓瘤成人患者的双抗药物。
Tecvayli双抗的作用靶点是BCMA和CD3。CD3是T细胞表面的一种跨膜抗原,表达B细胞成熟抗原(BCMA)是一种肿瘤相关抗原,在恶性骨髓瘤等肿瘤细胞表面高表达。
简单来说,Tecvayli双抗拥有两只手,一只靶向BCMA的手负责抓住癌细胞,另一只手负责将CD3阳性T细胞拽到癌细胞附近,使得其能够对癌细胞一招毙命。
在实际临床中,Tecvayli的表现也算可圈可点。在一项名为MajesTEC-1的 1/2 期临床试验中,纳入了165名患者多发性骨髓瘤患者,其中的104名患者在接受了五种治疗后,总缓解率仍然达到了63%。
值得一提的是,58.8%的患者获得非常好的部分缓解,39.4%患者出现了完全缓解。患者的中位无进展生存期为11.3个月,中位总生存期为18.4个月。
Tecvayli的出现,不仅仅意味着血液瘤患者的新希望,也意味着双抗赛道的热度和希望。
2022双抗爆发元年:1年获批上市产品超此前总和
实际上,Tecvayli已经是今年以来第五款获批上市的双抗药物。
今年1月份,在美国获批上市的Kimmtrak双抗,点燃了双抗领域的第一把火。
Kimmtrak既是第一款靶向gp100/CD3的新型T细胞受体(TCR)双抗疗法,也是第一个获得FDA批准用于治疗不可切除或转移性葡萄膜黑色素瘤的疗法。
还是在1月,FDA又批准了罗氏靶向Ang-2/VEGF-A的双抗药物Vabysmo,用于治疗新生血管性或湿性年龄相关性黄斑变性和糖尿病黄斑水肿。
Vabysmo也是第一个被批准用于眼部治疗的双特异性抗体。对与双抗领域来说,这也意味着双抗适应症不再被局限于血液瘤和实体瘤。
看起来,这两款双抗是不是已经很厉害了,但这还没完。
6月份,罗氏的CD20/CD3双抗药物Lunsumio在欧洲上市,成为了全球范围内的首款CD20/CD3单抗。在临床试验中Lunsumio也展示出了成为CAR-T疗法强力竞争对手的实力。
对于国内双抗玩家来说,更具有意义的应该是康方生物的双抗产品获批。
6月29日,康方生物的PD-1/CTLA-4双抗KN046获批上市,用于末线治疗宫颈癌。这是全球范围内,首个问世的PD-1/CTLA-4双抗。
过去,PD-1与CTLA-4联合用药对多个癌种都有不错的效果,不过联合用药的缺点是有着较为严重的不良反应。
而相比于联合疗法,PD-1/CTLA-4双抗则会更有效、更安全。而康方也成为了第一个吃螃蟹的人,为后来的国内玩家开辟了一条可行的路。
可以说,今年问世的双抗,都在刷新着双抗领域的天花板,也为双抗的未来带去了更多的想象空间。
如果拉长周期来看,2022年以来全球范围内获批上市双抗数量已,创造了历史新高。
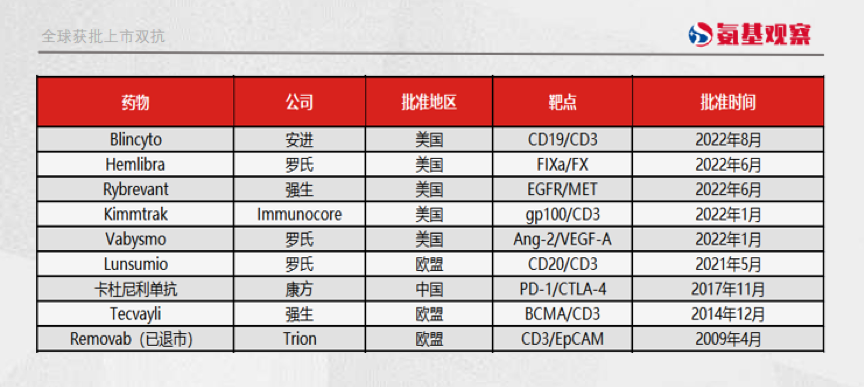
正如上图所示,在今年之前,获批的双抗也就4款。
双抗大爆发背后,技术瓶颈被打破
看到这里,你是不是也会有这样的疑问,从起步时间来看,双抗领域的起步并不算晚,那么为什么在过去的十几年间,双抗都发展缓慢,在今年却突然爆发了?
答案或许是,厚积薄发。
虽然双抗概念看似简单,似乎只要随意将两个抗体拼在一起,就能得到一个更强的创新药。但在实际研发过程中面临着诸多制约,技术上每向前走一步都无比艰难。
具体来说,此前在双抗领域的制约主要在于两方面,一是成药和产业化效率低,另一是药物半衰期短。
我们知道,双抗药物按照结构可以分为存在Fc区(可结晶区)的IgG样双抗和不含Fc区的非IgG样双抗。
对于存在Fc区的IgG样双抗来说,研发过程中的需要解决的是抗体结构错配问题,这就是链交换问题。也是因此,导致双抗产业化效率低、杂质蛋白多。
对于这一问题,全球不少大药企都推出了自己双抗技术平台,比如KiH、Crossmab、DuoBody等平台,通过这些平台双抗轻重链错配问题逐步得到解决。
而对于不含Fc区的非IgG样双抗来说,问题则在于半衰期较短。不含Fc区的非IgG样双抗分子量较小,易被靶细胞溶酶体降解,导致半衰期通常仅有两小时。Blincyto就是如如此,半衰期两小时,患者需要经常服药。这一点也成为了制约Blincyto销售的因素之一。
针对双抗的这一弊端,药企目前通过设计不同平台来提升双抗的半衰期来解决。曾经横在双抗研发领域的瓶颈,逐一被打破。也正因此,双抗迎来了丰收期。
总结
总而言之,正是由于过去几十年医学界不断的努力,将桎梏双抗的枷锁层层打破,如今我们才能看到双抗爆发式的成功。
不过,双抗未来仍有不少可以提升之处,比如针对实体瘤的探索。由于血液瘤药物的开发难度更低,目前双抗的大部分成就都是基于血液瘤。
但只有突破了实体瘤适应症,才能给给双抗的想象空间带来指数级别增长。就像DS-8201突破ADC的天花板一样。
但毋庸置疑的是,在双抗领域,同样的故事或许也将上演。随着双抗领域更多的药企涌入,天花板势必会不断被抬高。
仅在国内,包括康方生物、康宁杰瑞制药、百济神州、信达生物、恒瑞医药、宜明昂科、岸迈生物、友芝友等多家药企纷纷入局。
在即将开启的双抗的黄金时代,必然也少不了国内药企的身影。



评论