文|氨基财经 方涛之
有一种残忍的游戏叫做俄罗斯轮盘赌。
它的玩法很简单,只需要一把左轮手枪,然后在手枪的六个弹槽中装入一颗或多颗子弹,任意旋转转轮后,赌徒们将对准自己的头扣动扳机。
赌局结束,有倒霉蛋被“爆头”撒手人寰,也有幸运儿会赚得盆满钵满。
这种危险又诱人的游戏,在现实生活中并不多见,但在创新药研发领域却是屡见不鲜,因为创新药研发本就是一场运气和实力的双重较量。
这不,在CD73靶点研发领域,一场俄罗斯赌盘游戏已然开启。
作为肿瘤微环境的重要开关之一,CD73能够调控ATP-腺苷通路,恢复免疫细胞的免疫能力。也正因此,海外药企纷纷站上CD73的赌桌。
不过,既然是赌,总有输赢。随着这些药企的临床逐渐推进,临床数据将直接左右他们能否进入下一轮关卡。
回到国内,包括天境生物、康方生物、普米斯在内的多个玩家,也通过改良式创新的方式下注CD73赌局。
那么,在CD73赌桌上,谁会成为幸运儿呢?
/ 01 /被寄予厚望的肿瘤微环境“遥控器”
虽然尚未成药,但医学界广泛认为,阻断CD73通路是一种合乎逻辑的抗癌治疗策略。
这要从其机制说起。在人体内,CD73很重要的一个作用,是催化AMP(单磷酸腺苷)生成ADO(腺苷)。而ADO又会和腺苷受体A2A和A2B结合,抑制CD4+T细胞、NK细胞等多种免疫细胞的活性。
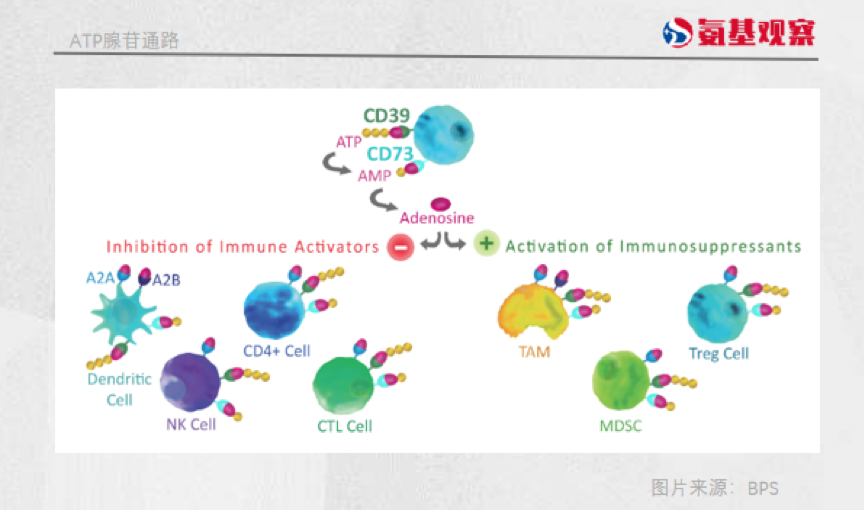
狡猾的肿瘤细胞正是利用了这一特点,上调自身CD73表达,增加腺苷的生成,来增强免疫逃逸。
因此,抑制CD73酶活性以减少腺苷生成,看上去是一个增强免疫细胞免疫反应可行方法。
虽然因为不利的靶结合位点等原因,CD73抗体单药表现出较弱的临床活性,却没有妨碍药企的研发热情。
原因在于,CD73与许多其它蛋白质一起在肿瘤微环境中过度表达,并且 CD73 抑制剂与靶向这些蛋白质的抗肿瘤剂的组合,可能是协同作用的。例如,CD73便有可能是PD-1的黄金搭档。
PD-1开启了免疫治疗的新时代,这是人尽皆知的故事。但硬币的另一面是,PD-1单药响应率较低,大约只有20%的患者适用。因此,从TIGIT到LAG-3,寻找PD-1黄金搭档,提高免疫治疗响应率的工作从未停止。
在这一背景下,CD73抑制剂的研发热情空前高涨。包括百时美施贵宝、礼来、阿斯利康、吉利德在内的不少大药企,其管线中都有着CD73抑制剂的身影。
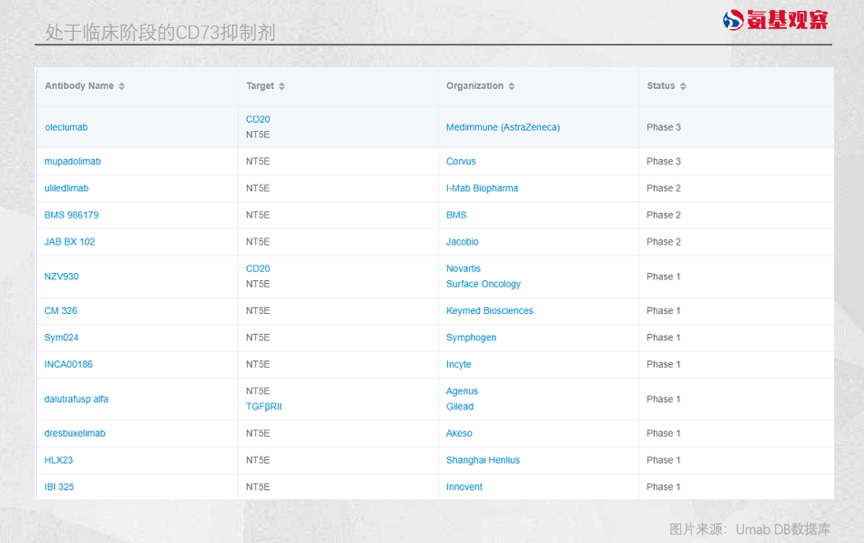
其中,“带头大哥”非阿斯利康莫属。在2021年ESMO大会上,阿斯利康CD73的2 期临床试验结果显示,对于NSCLC患者而言PD-L1单药客观缓解率18%,而CD73单抗Oleclumab联合PD-L1单抗客观缓解率30%。
在联合疗法效果实现翻倍的情况下,CD73+PD-L1安全性与PD-L1单药相似,这无疑给了CD73研发企业们更大信心。也正是凭借这一数据,阿斯利康在今年推进CD73单抗的三期临床研究工作。
某种程度上来说,也是这些带头大哥们进展顺利,进一步推动了CD73抑制剂的研发热潮。
/ 02 /带头大哥还未完全上岸
不过,火热归火热,CD73抑制剂研发现状是:革命尚未成功,同志还需努力。
进行CD73抑制剂研发的国际大药企,不少都吃了瘪,不是暂停临床试验就是调转临床研究方向。
比如说艺高人胆大的吉利德,此前开展了CD73/TGF-β双抗的研发。但目前,吉利德已经停止CD73/TGF-β双抗临床,转向CD73小分子抑制剂的开发。
碰壁的还有百时美施贵宝。2021年一季度,百时美施贵宝将CD73单抗BMS-986179从临床活跃管线中移除。
大药厂们接连调整方向也不奇怪,新药研发总是充满不确定性,疗效或安全性往往是问题所在,CD73抑制剂也是如此。
疗效方面,正如上文所说,由于不利的靶结合位点和酶抑制机制等众多原因导致,CD73抑制剂要想做出效果需要两把刷子;与此同时,CD73在各种组织中的多种细胞类型上普遍表达,因此还要平衡毒副作用问题。
百时美施贵宝终止研发的原因,便是因为没有找到平衡之道。其CD73单抗BMS-986179在单药存在毒副作用较大的情况下,调整临床策略转向联合疗法。但联合疗法也没能解决这一问题,不得不放弃赌局。
时至今日,即便是CD73抗体药物研发带头大哥阿斯利康也未上岸。
虽然公司此前公布的2期临床数据惊艳,但阿斯利康在今年8月公布的一项名为HUDSON的伞式临床试验数据显示,其CD73抑制剂似乎遭遇挑战。
这项实验评估了阿斯利康的PD-L1与几种不同药物联用治疗非小细胞肺癌的效果,其中包括CD73与PD-L1的联合疗法。
结果显示,CD73联用PD-L1没能对接受PD-L1治疗并出现进展的患者,展现更好的疗效优势。
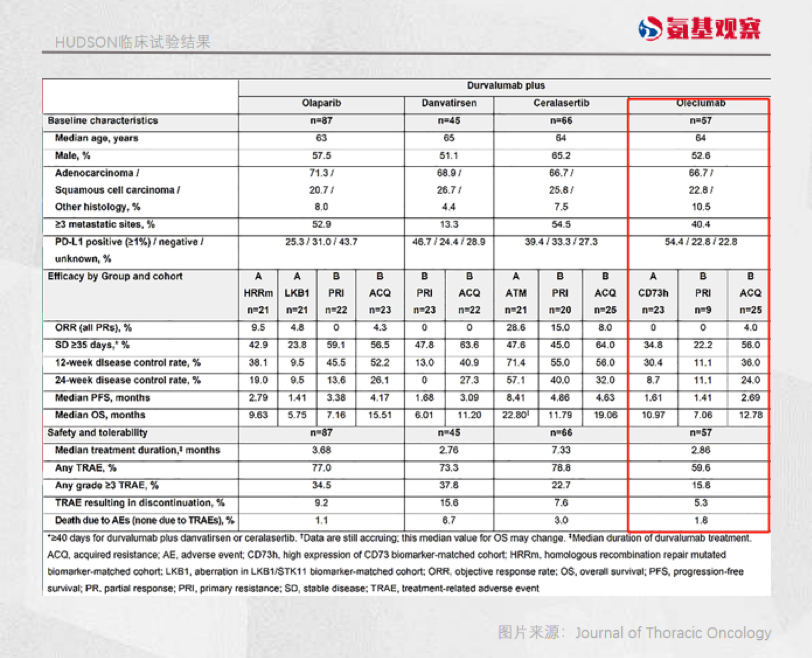
虽然在这项临床试验并非“金标准”的大样本随机双盲实验,并不能因此就给其CD73抑制剂判“死刑”,但其背后透露出来的危险信号仍然值得关注。
/ 03 /国内玩家谁能弯道超车?
未来,任何一家企业在CD73研发领域遭遇失败,我们都不用感到奇怪。
一方面,这一信号通路机制仍然不够明确。虽然抑制CD73能够抑制大部分肿瘤的生长,但对另一些癌症来说可能并非如此。一些研究已经表明,高 CD73 表达与乳腺癌患者的预后无关,甚至高CD73表达与胃癌或直肠腺癌患者的良好预后相关。
另一方面,药企们研发的分子也可能存在Bug。例如,阿斯利康的CD73单抗存在一个明显的问题:“钩子效应”。钩子效应指的是:
药物会在某个浓度下达到最大效果,后续药量继续增高药效反而会下跌。这是因为阿斯利康CD73单抗Oleclumab的结合位点结构所导致。
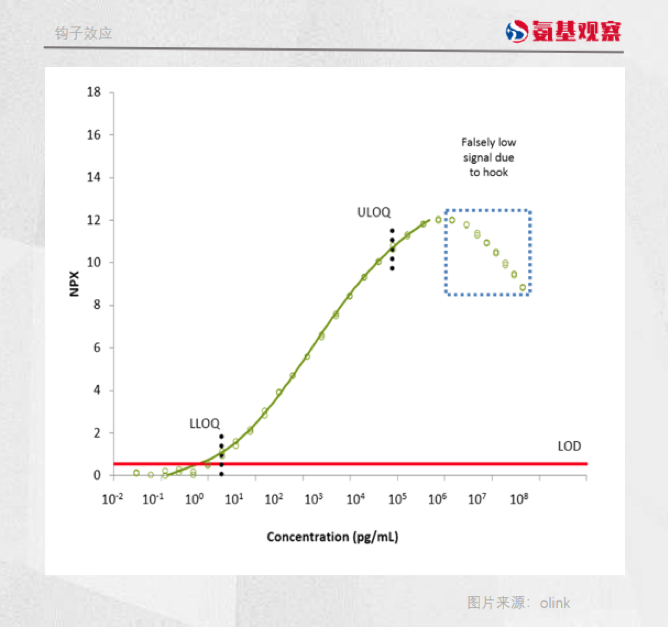
CD73单抗研发对于抗体抗原的比例要求极为苛刻,一旦抗原抗体比例不合适,便会产生钩子效应。对于国内企业来说,这是挑战,但也是机会。目前,国内药企也在不断朝着改进方向前进。
例如天境生物、普米斯生物都采用了差异化的CD73结构设计避免“钩子效应”。
拿天境生物来说,其CD73单抗与CD73二聚体的C端结构域单价结合,从而完全抑制CD73的酶活性,不引起钩子效应。
还有药企希望通过开发双抗的方式解决这一问题。例如,康方生物研发了PD-1/CD73双抗,这种结构既能够完全抑制CD73的酶活性,又能阻断PD-1介导的免疫细胞抑制,起到一箭双雕的作用。
无论国内药企对CD73抑制剂的改进结果如何,国内创新药行业的进步都是肉眼可见的。
在这个过程中,药企们可能会失败。随着国内药企持续推进CD73抑制剂的研发,也必不可免接受后期临床数据的考验。
但不管怎么说,受挫是药企的必经之路。也只有经过淬火历练,中国创新药企才能成为真正具备创新能力的创新药企。



评论