文|氨基观察
在创新药世界,所有人都希望做大做强。
过去几年的PD-1热潮,就是最好的印证。数十年难得一遇的广谱大靶点,带来极高的想象空间,驱使着药企们不断入局。
但再大市场,也架不住内卷的挤压,大靶点,最终变成了小市场。
“内卷”,不仅在PD-1,更在于其它大靶点。这使得biotech的生存空间不断被挤压。但与此同时,整个国内创新药生态也在不断发生变化。
Biotech开始主动追求“做小”,在“夹缝”中求生。当前申报科创板IPO韬略生物就是这样一个例子。其核心管线主打错位竞争,针对罕见的基因突变群体。

对于韬略生物来说,虽然核心管线针对的患者群体规模有限,最终限制了天花板。但凡事有利有弊,这一策略也能因为满足临床未满足需求的特殊性,加快临床进度。
对于biotech来说,这未尝不是一个可行的策略。
虽然尚未有管线上市,但韬略生物的梦想并不小,其在科创板上市期望的融资估值是100亿。那么,韬略生物能够圆梦吗?
01 “夹缝”中求生
创新药研发如何以差异化取胜?答案不尽相同,更好的安全性、更低的副作用、更优的依从性……相比现有药物,任一维度的改善,都称得上是差异化。
除此之外,更大的差异化竞争,是走没有人走的路。比如,在夹缝中求生的韬略生物。韬略生物的核心管线有3个,分别是苏特替尼、TL118、克耐替尼。
这3个管线,都称得上是夹缝中求生——同类机制药物难以触及的患者群体。
首先来看苏特替尼,这是一款EGFR-TKI。当前,市面上已经有多款EGFR-TKI上市。不过,苏特替尼针对的是两类特殊群体。
一类是非耐药性的非典型突变群体,比如不常见的L861Q、G719X、S768I突变患者群体;
另一类则是第三代EGFR一线治疗后耐药的非典型突变群体。
对于TKI来说,天然的弱点是耐药性。为了应对耐药性问题,EGFR-TKI从一代升级到如今的三代,四代药物的竞争也已经打响,即满足三代EGFR-TKI耐药患者的需求。
不过,苏特替尼的针对的三代耐药非典型突变的患者群体,即与主流的四代EGFR-TKI形成错位竞争。
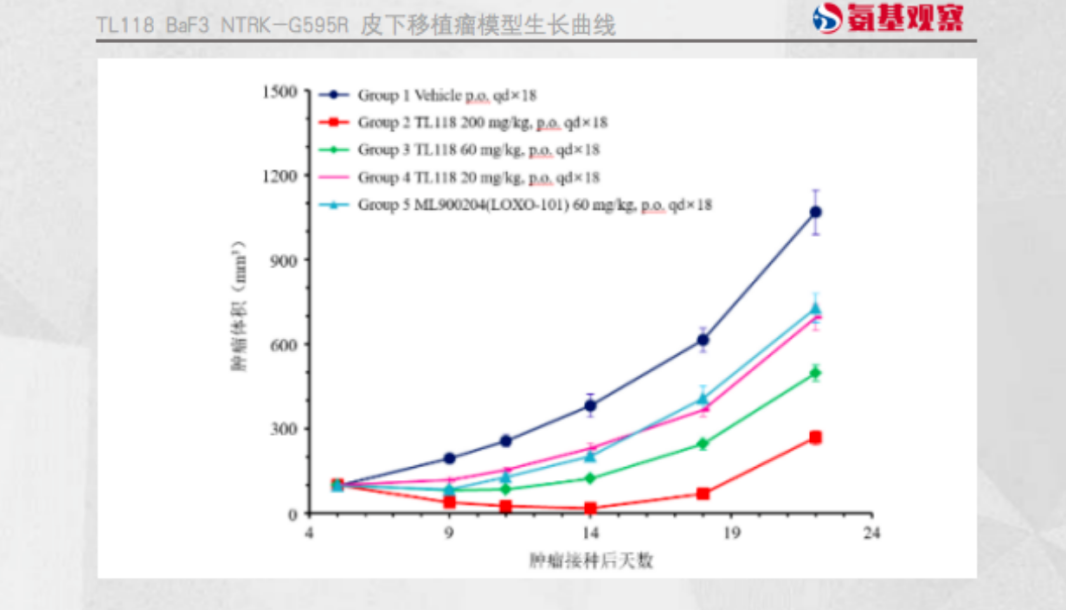
再来看TL118。TL118是一款TRK小分子抑制剂。当前,市面上已有拉罗替尼和恩曲替尼等同类药物上市,TL118主要针对现有药物的耐药群体。根据公司招股书,TL118有较高的针对耐药性突变的抑制活性。
最后来看克耐替尼。克耐替尼一款EGFR/BTK双靶点抑制剂。与苏特替尼不同,其不针对特定突变的群体,而是针对经EGFR抑制剂治疗后,脑转移或脑转移进展的晚期非小细胞肺癌患者,主要解决癌细胞中枢神经系统远端转移的问题。
就当前来说,肺癌中枢神经系统转移也是预后效果最差的肺癌并发症之一,缺乏有效的治疗手段,患者的自然生存期仅为1-2个月。
总的来说,韬略生物的策略就是,避开现有药物的锋芒,而是在“夹缝”中寻找自己的机会。
那么,该如何看待这一策略呢?
02 牺牲与所得
从临床推进角度来说,这一策略能够节省时间成本,加快研发进程。核心原因在于,韬略生物研发药物针对的适应症,大部分都未有药物上市,因此能够单臂研究申报上市。
所谓单臂研究,指的是即单组临床试验。顾名思义,就是仅有一个组的研究,没有为试验组设计相对应的对照组,或者对照试验为其本身。
与之对应的是双臂研究。即为两组试验,病例组和对照组,通常两组需要“双盲”,研究者和病人均无法得知所在的小组。
相较于双臂研究,单臂研究更为简单,省时省力,通常只是作为探索性试验。正常情况下,只有经过多臂、双盲的临床试验得出来的数据,才会被监管认可。
但CDE规定,在满足临床未满足需求的情况下,研发药物可以通过单臂试验结果获得有条件上市,后续再开展确证性临床试验,也就是先上车后买票。
当前,苏特替尼开展的所有3项临床,都为单臂研究;TL118在美国开展针对儿童晚期实体瘤的适应症也是单臂研究。
不过,凡事都有两面性。韬略生物的策略是避开主流药物锋芒,也因此失去了主要的患者群体。
例如,苏特替尼进展最快的适应症为,针对携带非耐药性EGFR非经典突变(L861Q、G719X 和/或 S768I)的局部晚期或转移性非小细胞肺癌患者。根据招股书,我国该类患者群体约为3万人,理想情况下的销售峰值约为5亿元。
国内如此,海外也是这样。
在美国非小细胞癌领域,携带非耐药性EGFR非经典突变(E709A、E709K、R776H、G724S、G779F等)的群体,加上携带经第三代EGFR抑制剂一线治疗后产生的耐药性非经典突变患者群体规模,只有约3100人。
在这一背景下,苏特替尼必然没有施展拳脚的大空间。
生存空间更窘迫的是TL118。根据招股书,TL118针对NTRK基因融合阳性的群体,中国销售收入峰值大约为3.3亿元。若届时其主要针对现有药物的耐药患者群体,销售费峰值将会进一步下降。
很显然,在选择临床加速、竞争较弱等优势的同时,韬略生物也主动让出了大部分创新药市场。
03 现在与未来
小biotech也有大梦想。
根据上交所官网,韬略生物融资规模预计为10.73亿元,对应发行的股本不超过10%。按照该数字计算,韬略生物上市的期望估值超过100亿元。
目前,除了苏特替尼、TL118、克耐替尼,韬略生物其它管线包括HER2小分子抑制剂等,面临研发过于早期以及赛道竞争过于激烈的问题,未来充满不确定性。
这意味着,韬略生物虽然仅处于“VC”阶段,但已然把成熟阶段的预期全部释放。
不过,从产业发展角度来说,我们无疑应该鼓励更多像韬略生物这样的选手出现。
过去几年,创新药环境虽然得到了极大的改善,临床研究也如雨后春笋般涌现。
但大部分都是同质化的竞争,存在低水平重复的情况,浪费临床资源。这也是为什么,国内创新药领域现阶段被人诟病大而不强。
而Biotech的本质是勇于向无人区挺进。只有这样,才能促进整个创新生态的良性循环。
换句话说,当越来越多像韬略生物这样的企业出现,才真正意味着,中国创新药行业又往前迈进了一大步。




评论