文|氨基观察
技术大航海时代,老靶点、新机遇成常态,CD20靶点就是如此。
缔造全球第一款治疗肿瘤的单抗靶点,CD20堪称传奇,罗氏的利妥昔在该领域曾创下年收入70亿美金的纪录。
如今,利妥昔已老,但CD20的新故事还在继续。以罗氏为首的药企们,对CD20靶点发起了一场升级战,使得该领域进入CD3/CD20双抗之争。
过去一年,罗氏、艾伯维一共三款CD3/CD20双抗上市,预示着大战的开始。但竞争还未结束,后续包括再生元、诺诚健华等国内外药企,也将加入战场。
那么,CD20靶点的新故事,主角将会是谁呢?
/ 01 / CD20靶点的升级赛
从利妥昔开始,为了达到更好的效果,CD20靶点的升级赛从未停止,单抗就经过了3代更迭。不过,利妥昔依然是当之无愧的王者。因为,第二代和第三代产品,都没有真正打败利妥昔。
但在创新技术不断出现的情况下,超越者终于出现了。2022年6月8日,罗氏的CD3/CD20双抗Mosunetuzumab在欧洲获批上市,CD20靶点之争正式进入双抗时代。
与单抗相比,双抗是一个全新机制的升级。CD20单抗通过补体与抗体依赖性细胞毒性杀伤目标细胞,而双抗则是通过牵引T细胞的方式进行打击。
Mosunetuzumab的作用机制,是B细胞表面的CD20和T细胞表面的CD3。简单理解,就是一只手抓住T细胞,另一只手将肿瘤细胞抓到T细胞面前,使T细胞定向杀伤肿瘤细胞。
因为血液中含有丰富的T细胞,并且还可以轻松接触“致病”的肿瘤细胞,两者结合,强效杀敌。这也是CD3/CD20双抗在血液瘤中拥有较好效果的原因。
临床数据显示,Mosunetuzumab治疗至少接受过两种全身治疗的复发或难治性(R/R)滤泡性淋巴瘤(FL)患者,客观缓解率(ORR)高达80%,其中60%达到完全缓解。
效果到底有多好呢?可以对比利妥昔单抗在同适应症的结果。如下图所示,Mosunetuzumab的客观缓解率是利妥昔的1.6倍,而治疗更具深度的指标完全缓解率则是后者的7倍。
总的来说,Mosunetuzumab表现出了更有深度和更持久的缓解。凭借优秀的临床表现,Mosunetuzumab迅速获得了认可。去年12月23日,FDA加速批准了Mosunetuzumab的上市,用于治疗经过两线或更多线全身治疗后的R/R FL成年患者。
/ 02 / 开始角逐的大擂台
不过,在罗氏领衔CD20靶点的升级赛的同时,竞争对手也在加速进入市场。
今年5月,艾伯维的CD3/CD20单抗Epkinly,获得FDA的加速审批,成为首款用于治疗DLBCL(弥漫大B细胞淋巴瘤)患者的双抗,与Mosunetuzumab形成了错位争锋的姿态。
不过,从适应症人数来看,相比于Mosunetuzumab,Epkinly机遇更大。如下图所示,Epkinly的DLBCL,是淋巴瘤适应症最大的群体。
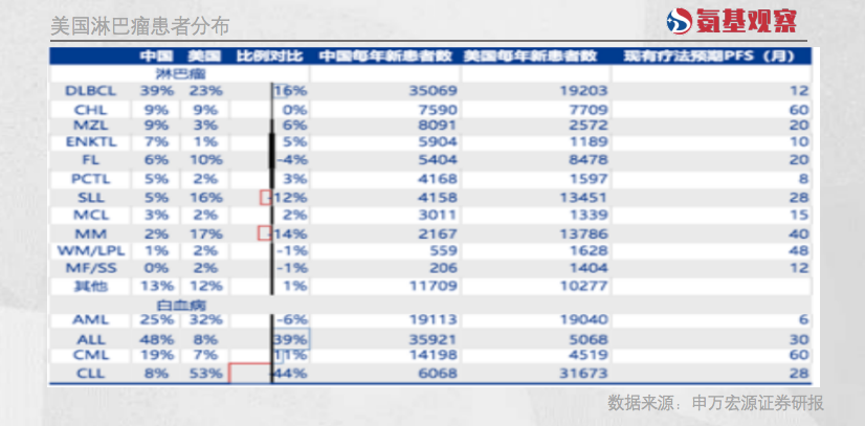
但很显然,巨大的市场并不会被艾伯维独享。6月15日,罗氏的第二款CD3/CD20双抗Columvi,获得FDA批准上市,用于治疗经过二线或多线的系统治疗的R/R DLBCL,或由滤泡性淋巴瘤引起的大B细胞性淋巴瘤(LBCL)成年患者。
与Mosunetuzumab相比,罗氏对Columvi进行了一番优化,设计为非对称型结构,Fab区与CD20二价结合,与CD3单价结合。
这种独特的结构使得Columvi对CD20的结合活性更高,在效应细胞与靶细胞比例较低情况下也能有效杀伤B细胞。同时,位于内部CD3的结合位点,与T细胞的结合作用被抑制,可以防止T细胞过度激活。
临床结果显示,在R/R DLBCL患者中,33%接受过CAR-T细胞疗法,接受Columvi的患者ORR为56%,CR为43%,mDOR为18.4个月。
不过,这是否能够让Columvi后来居上不得而知,毕竟Columvi并不能够证明其优于Epkinly。接下来,双方的缠斗将会继续。目前,双方均在进一步推进双抗与标准疗法的联合治疗探索。
在罗氏和艾伯维的角逐之下,CD3/CD20双抗的发展将会加速推进。这,或许也将吸引更多参战者入局。
/ 03 / 谁能成为新主角?
除了领跑的罗氏和艾伯维,CD3/CD20双抗领域后起之秀们正迅速崛起。
据新药数据库统计,在两家公司之后,目前已经有11款CD3/CD20双抗进入临床,其中最快的是再生元的Odronextamab,已经进入Ⅲ期临床阶段。
去年的ASH会议上,再生元公布了Odronextamab的Ⅱ期临床数据,在未尝试过CAR-T疗法的大B细胞淋巴瘤患者,ORR为49%,CR为30.8%,mDOR为10.2个月。
在CD20的新赌桌上,国内药企必然不会缺席。早在3年之前,再鼎医药斥资1.9亿美元将其引进,如今Odronextamab正在国内开展Ⅱ期临床试验。
其他的国内企业也不甘落后,包括诺诚健华、嘉和生物、天广实、君实生物等企业的CD3/CD20双抗,均进入临床试验阶段。
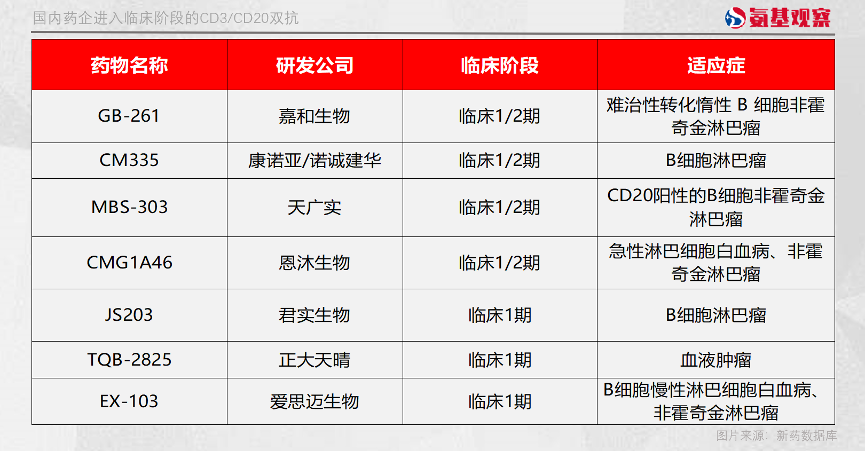
对于这些后来者来说,未尝没有突围的机会。除了在疗效方面超越之外,安全性层面也有突围方向。
通过引导T细胞靶向表达CD20的恶性B细胞的过程中,这一组合可能会引起一种免疫过度反应,由此引发细胞因子综合征(CRS)和免疫效应细胞相关神经毒性综合征 (ICANS)。已上市的三款CD3/CD20双抗药物,也都因此都被FDA标以黑框警告。
因此,如何提高疗效的同时降低副作用,是后来者的机遇。当然了,更是都是挑战。尤其是国内药企的CD3/CD20双抗仍处于临床早期,前景也会更充满变数。
胜利者固然可以占据百亿美金市场,但失败者也会付出代价。入局的国内药企,要加油了。



评论